actividad inicial
la motivacion
la motivacion es muy importante a la hora de realizar trabajos o en tu vida, esto puede ser muy dificil pero si tienes mucha motivacion y dedicacion, por ejemplo a la hora de escoger una profesion esta tiene que ser una que nos motive, para realizarla con mas pasion y esta resulta mas facil.
caracteristicas de los gases
Sus partículas no están unidas: los gases es que las partículas o moléculas que los componen no están unidas ni atraídas entre sí. Se diferencian de los sólidos, en los cuales las moléculas están unidas y no intercambian su posición entre sí.Las partículas dentro de los gases se encuentran en un estado de caos en el que la gravedad no tiene ningún efecto en ellas. No presentan un desorden absoluto, pero sí en gran medida.
No tienen forma definida:Al estar las partículas del gas dispersas entre sí, las distancias que las separan entre ellas son sumamente grandes en comparación con el tamaño de las mismas.Esta propiedad produce que los gases tiendan a ocupar todo el espacio del recipiente en el que se encuentren, adquiriendo su misma forma. El gas no tiene una forma definida, porque por su naturaleza adquiere la forma del espacio en el que se encuentre.Al ingresar una masa gaseosa dentro de un contenedor de cierto tamaño y forma, sus partículas, en estado de desorden y moviéndose a gran velocidad, pasarán a abarcar todo el espacio dentro de él para continuar en su mismo estado.
Ocupan mayor volumen que los sólidos y líquidos: Como producto de todas las propiedades anteriormente mencionadas, los gases también tienen la característica de que ocupan un mayor espacio –o poseen un volumen mayor- que los sólidos y los líquidos.Los sólidos tienen un volumen propio, es decir, su volumen está determinado por sus mismos componentes, que no cambian de posición
Tienen baja densidad: Recordemos que la densidad es la masa que existe en una unidad de volumen. Al estar las moléculas que conforman la materia gaseosa separadas y dispersas entre sí, la cantidad de moléculas –o de materia- existente en una cantidad de volumen determinada es mucho menor que en los estados líquidos y sólidos.
Son fácilmente comprimibles:Como en los gases las moléculas tienen una gran distancia que las separa unas de otras, pueden ser comprimidos con gran facilidad –a diferencia de los sólidos
Existen diferentes tipos
Algunos tipos de gases, clasificados de acuerdo a su uso, son los siguientes:
- Gases combustibles: son aquellos gases cuyos componentes funcionan como combustibles, por lo cual son utilizados para la producción de energía térmica. Algunos de ellos son el gas natural, el gas licuado de petróleo y el hidrógeno.
- Gases industriales: son aquellos gases manufacturados, que se comercializan al público para distintos usos y aplicaciones, como por ejemplo para los sectores de la salud, la comida, protección ambiental, metalurgia, industria química, seguridad, entre otros. Algunos de estos gases son el oxígeno, nitrógeno, helio, cloro, hidrógeno, monóxido de carbono, propano, metano, óxido nitroso, entre otros.
- Gases inertes: son aquellos gases que bajo condiciones de temperatura y presión específicas, no generan ninguna reacción química o una muy baja. Son el neón, argón, helio, kriptón y el xenón. Se utilizan en procesos químicos en los que son necesarios elementos no reactivos.
TEMPERATURA
es una propiedad de los cuerpos que nos da idea del mayor y menor grado de agitación que posee las moléculas.Cuando se trabaja con gases se utiliza la temperatura absoluta.
CANTIDAD DE UN GAS
la masa del gas se puede medir en gramos,kilogramos,y moles en gas.
VOLUMEN
como un gas llena completamente el recipiente que lo contiene,litros,metros cúbicos ,unidades de volumen.
GAS IDEAL
Un gas ideal es un compuesto ,de un conjunto de partículas puntuales con desplazamiento aleatorio que no interactúan entre si.
LEYES DE LOS GASES

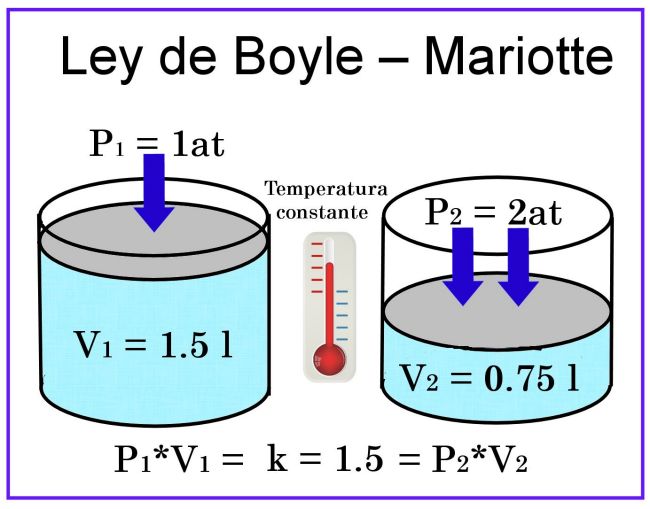
Ley de Boyle. “El volumen de un gas varía de forma inversamente proporcional a la presión si la temperatura permanece constante.” Se expresa según la fórmula: P1xV1 = P2xV2.
Ley de Gay-Lussac. Explica que la presión de una masa de gas cuyo volumen se mantiene constante es directamente proporcional a la temperatura que posea. Esto se formula de la siguiente manera: P1/T1 = P2/T2.

Ley de Charles. Expresa la relación constante entre la temperatura y el volumen de un gas, cuando la presión es constante. Su fórmula es: V1 / T1 = V2 /T2.

Ley de Avogadro. “En iguales condiciones de presión y temperatura, las densidades relativas de los cuerpos gaseosos son proporcionales a sus números atómicos”.

ACTIVIDAD INICIAL LA TIERRA
debemos saber que la tierra esta sufriendo deforetaciones masivas de arboles, contaminacion masiva en los rios, a que cada ves estan poblando lugares que no se pueden por su geografia, estamos acabando con nuestro planeta y cada ves este esta mas poblado.



No hay comentarios.:
Publicar un comentario