ACTIVIDAD INICIAL EL GRAFENO
El grafeno es un material proveniente del grafito y surge cuando las partículas del carbono se agrupan de forma densa en láminas con forma hexagonal. El grafeno es, además, el material más fuerte que existe
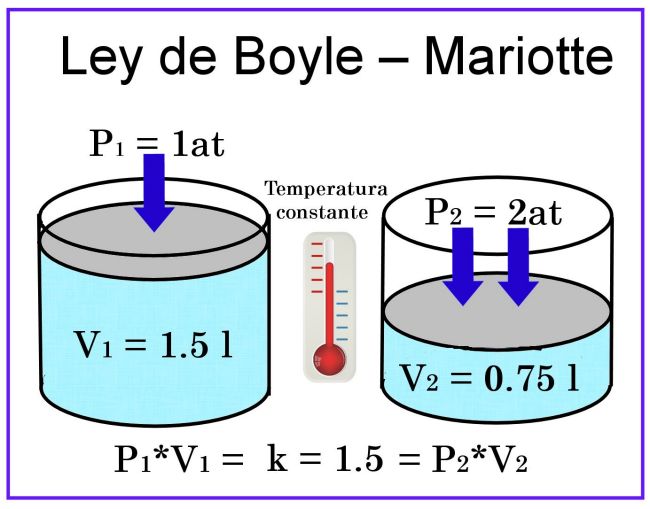
LEY DE GRAHAM.
Consiste en la investigación de la difusión de los gases y que los gases mas livianos se difunden mas rápido y que los menos livianos se demoran mas.El fenómeno de efusión está relacionado con la energía cinética de las moléculas. Gracias a su movimiento constante, las partículas de una sustancia se distribuyen uniformemente en el espacio libre.
por ejemplo
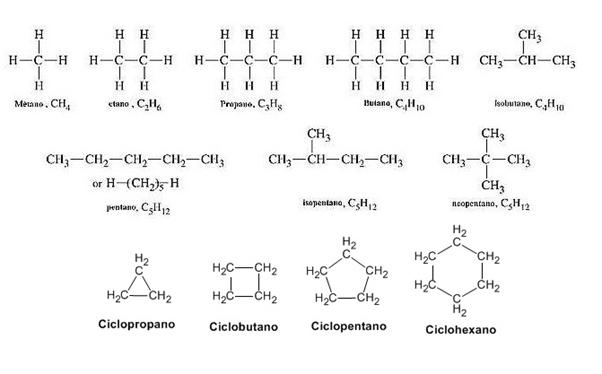
COMPUESTO ORGANICO
Son todos aquellos compuestos químicos los cuales su estructura está formada a base de carbonos enlazados entre sí. La principal característica de estos compuestos es que son combustibles por lo que es necesario trabajar lejos de cualquier tipo de llama. La mayoría de los compuestos orgánicos se producen de forma artificial mediante síntesis química aunque algunos todavía se extraen de fuentes naturales.
COMPUESTOS INORGANICOS
A diferencia de los orgánicos, típicos de la química de la vida, los compuestos inorgánicos son aquellos cuya composición no gira en torno al carbono y al hidrógeno, sino que involucra diversos tipos de elementos, casi todos los conocidos de la tabla periódica.
FORMAS ALOTRÓPICAS DEL CARBONO
Grafito:
El grafito posee una estructura laminar (como se puede observar en la figura), las láminas están separadas por capas, y cada capa tiene una separación entra ellas de 3.35 Å, que se corresponde a la suma de los radios de Van der Waals, lo que nos indica que las fuerzas entre las capas debe de ser relativamente débil. Este hecho nos indica la blandura del grafito, así como las propiedades lubricantes, que se suele atribuir al deslizamiento de una capa sobre la otra.
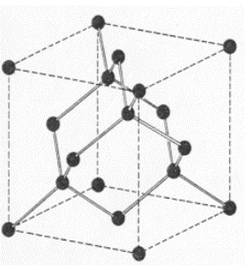
Diamante:
El diamante tiene una estructura de cristal covalente tridimensional, que se encuentra formado por enlaces C-C interconectados, extendiéndose a través de todo el cristal, por lo que se dice que el diamante es una molécula gigante. La estructura cristalina, es cúbica y se encuentra centrada en la cada, a dicha estructura se la conoce comúnmente como red de diamante.
FULLERENO
Se forman cuando el grafito se vaporiza en un láser. Esta es una variedad de grupos, grandes que tienen un núcleo constante de átomos de carbono.
NANOTUBOS DE CARBONO
Los nanotubos de carbono de pared simple (SWCNT – Single Wall Carbon Nanotubes) están constituidos por átomos de carbono dispuestos en una red hexagonal cilíndrica, de forma que su estructura es la misma que se obtendría si se enrollara sobre sí misma una lámina de grafito.